
Estelionato
saúde
Sistema da agência registrou 2.436 eventos adversos desde 2018; notificações envolvem medicamentos usados para diabetes e obesidade.

Escrito por Redação em 23 de fevereiro de 2026
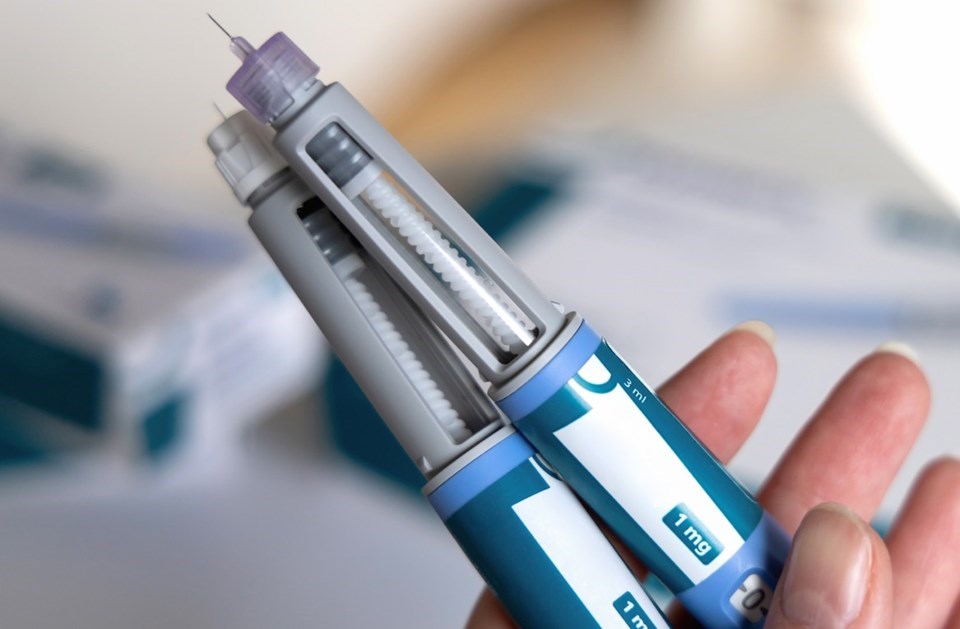
A Agência Nacional de Vigilância Sanitária (Anvisa) investiga 65 notificações de mortes suspeitas associadas ao uso de canetas emagrecedoras no Brasil. Os registros foram feitos entre 1º de dezembro de 2018 e 7 de dezembro de 2025.
No mesmo período, o sistema Vigimed, banco oficial de farmacovigilância da agência, recebeu 2.436 notificações de eventos adversos relacionados a esses medicamentos. Os dados envolvem quatro princípios ativos: semaglutida, liraglutida, dulaglutida e tirzepatida.
Essas substâncias são indicadas para o tratamento de diabetes tipo 2. Algumas formulações também têm autorização para uso contra a obesidade. No mercado brasileiro, estão presentes em marcas como Ozempic, Wegovy, Mounjaro, Saxenda, Victoza, Trulicity, Rybelsus e Xultophy.
A Anvisa destaca que uma única notificação pode reunir mais de um evento adverso. Também pode incluir mais de um desfecho clínico. Por isso, o registro no sistema não comprova que o medicamento tenha causado a morte.
Para confirmar relação causal, a agência exige avaliação clínica e científica detalhada. A análise considera o estado de saúde do paciente, o uso de outros medicamentos, a qualidade das informações enviadas e a regularidade do produto utilizado.
Entre os eventos adversos notificados, a pancreatite aparece com destaque. A agência contabilizou 145 registros da complicação. Em dados de pesquisas clínicas, o número chega a 225 ocorrências. Seis mortes foram relatadas em casos que envolvem pancreatite.
A Anvisa afirma que as bulas desses medicamentos já informam sobre a possibilidade desse tipo de complicação. A agência também diz que não é possível identificar, com base nas notificações, se os casos envolvem produtos regularizados, manipulados ou importados sem registro.
Parceria entre Prefeitura e UVV amplia acesso a consultas
O sistema Vigimed funciona como ferramenta de monitoramento após a comercialização dos medicamentos. Profissionais de saúde, pacientes e empresas podem relatar eventos adversos. O objetivo é identificar sinais de segurança e orientar possíveis medidas regulatórias.
A existência de notificações, no entanto, não significa que os medicamentos sejam inseguros e não comprova, por si só, que tenham provocado os óbitos registrados.